Khí butan C4H10 có trong thành phần khí dầu mỏ. Tính thể tích khí oxi (đktc) cần để đốt cháy 2,9 gam butan và tính số gam nước tạo thành sau phản ứng. Biết sản phẩm của phản ứng đốt cháy C4H10 là CO2 và H2O.

Những câu hỏi liên quan
Tính thể tích khí O2(đktc) cần dùng để đốt cháy hoàn toàn 7,4 gam hỗn hợp khí metan và khí butan(C4H10). Biết rằng sau phản ứng người ta thu được 22 gam khí CO2
16nmetan+58nbutan=7,4 (1).
BT C: nmetan+4nbutan=22/44=0,5 (2).
Giải hệ phương trình gồm (1) và (2), ta suy ra nmetan=0,1 (mol) và nbutan=0,1 (mol).
Số mol nước tạo ra là 0,5.(0,1.4+0,1.10)=0,7 (mol).
BTKL: 7,4+32nkhí oxi=22+0,7.18, suy ra nkhí oxi=0,85 (mol).
Thể tích khí oxi cần tìm là 0,85.22,4=19,04 (lít).
Đúng 1
Bình luận (2)
\(n_{CO_2}=\dfrac{22}{44}=0,5mol\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_4H_{10}}=y\end{matrix}\right.\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x 2x x ( mol )
\(2C_4H_{10}+13O_2\rightarrow\left(t^o\right)8CO_2+10H_2O\)
y 13/2 y 4y ( mol )
Ta có:
\(\left\{{}\begin{matrix}16x+58y=7,4\\x+4y=0,5\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\Rightarrow n_{O_2}=2.0,1+\dfrac{13}{2}.0,1=0,85mol\)
\(V_{O_2}=0,85.22,4=19,04l\)
Đúng 0
Bình luận (3)
Khí butan ( C4H10) là thành phần chính của khí gaz. Đốt cháy một lượng khí butan bằng 1456 ml Oxi ( lấy vừa đủ) thí sau phản ứng thu được khí Cacbonic và hơi nước.a. Lập PTHH của phản ứng trênb. Tính khối lượng sản phẩm khí thu được và thể tích khí butan bị đốt cháy.c. Tính thể tích khí Gaz cần lấy, biết butan chiếm 80% thể tích khí Gaz.Các thể tích khí đo ở ĐKTC
Đọc tiếp
Khí butan ( C4H10) là thành phần chính của khí gaz. Đốt cháy một lượng khí butan bằng 1456 ml Oxi ( lấy vừa đủ) thí sau phản ứng thu được khí Cacbonic và hơi nước.
a. Lập PTHH của phản ứng trên
b. Tính khối lượng sản phẩm khí thu được và thể tích khí butan bị đốt cháy.
c. Tính thể tích khí Gaz cần lấy, biết butan chiếm 80% thể tích khí Gaz.
Các thể tích khí đo ở ĐKTC
\(n_{O_2}=\dfrac{1456:1000}{22,4}=0,065\left(mol\right)\\ a,2C_4H_{10}+13O_2\rightarrow\left(t^o\right)8CO_2+10H_2O\\ b,n_{CO_2}=\dfrac{8}{13}.0,065=0,04\left(mol\right)\\ n_{H_2O}=\dfrac{10}{13}.0,065=0,05\left(mol\right)\\ b,m_{sp}=m_{CO_2}+m_{H_2O}=44.0,04+18.0,05=2,66\left(g\right)\\ c,n_{C_4H_{10}}=\dfrac{2}{13}.0,065=0,01\left(mol\right)\\ V_{gas}=\dfrac{100}{80}.0,01.22,4=0,28\left(l\right)\)
Đúng 1
Bình luận (0)
Bài 2. Đốt cháy 34,8 gam butan C4H10 trong bình chứa 89,6 lít khí oxi (đktc). Phản ứng xảy ra theo sơ đồ sau:
C4H10 + O2 -----> CO2 + H2O
a) Chất nào còn dư sau phản ứng? Khối lượng bằng bao nhiêu gam?.
b) Tính thể tích khí CO2 (đktc) và khối lượng H2O tạo thành sau phản ứng
Đốt cháy hoàn toàn 3,7 gam hỗn hợp khí Z gồm metan và butan C 4 H 10 . Sau khi kết thúc phản ứng, thu được 11 gam khí C O 2 . Tính thành phần phần trăm theo khối lượng mỗi khí trong hỗn hợp ban đầu.
Bình đựng ga dùng để đun nấu trong gia đình có chứa 12,5 kg butan
C
4
H
10
ở trạng thái lỏng, do được nén dưới áp suất cao.Tính thể tích không khí cần ở đktc dùng để đốt cháy hết lượng nhiên liệu có trong bình ( biết oxi chiếm khoảng 20% thể tích không khí, phản ứng cháy butan cho
C
O
2
và
H...
Đọc tiếp
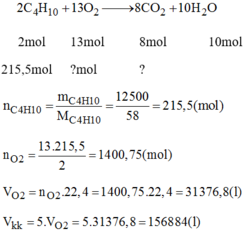
Bình đựng ga dùng để đun nấu trong gia đình có chứa 12,5 kg butan C 4 H 10 ở trạng thái lỏng, do được nén dưới áp suất cao.
Tính thể tích không khí cần ở đktc dùng để đốt cháy hết lượng nhiên liệu có trong bình ( biết oxi chiếm khoảng 20% thể tích không khí, phản ứng cháy butan cho C O 2 và H 2 O ).
Tính khối lượng khí oxi cần dùng để đốt cháy hoàn toàn 9.62 g hỗn hợp khí metan(CH4)và khí butan (C4H10).biết rằng sau phản ứng dụng người ta thu được nước và 28.6 g khí co2
Butan có công thức C4H10 khi cháy tạo ra khí cacbonic và hơi nước, đồng thời tỏa nhiều nhiệt. Hãy tính thể tích khí oxi cần dùng để đốt cháy 6,72 lít khí butan
Theo gt ta có: $n_{C_4H_{10}}=0,3(mol)$
$C_4H_{10}+\frac{13}{2}O_2\rightarrow 4CO_2+5H_2O$
Ta có: $n_{O_2}=1,95(mol)\Rightarrow V_{O_2}=43,68(l)$
Đúng 4
Bình luận (0)
\(n_{C_4H_{10}} = \dfrac{6,72}{22,4} = 0,3(mol)\\ C_4H_{10} + \dfrac{13}{2}O_2 \xrightarrow{t^o} 4CO_2 + 5H_2O\\ n_{O_2} = \dfrac{13}{2}n_{butan} = 1,95(mol)\\ \Rightarrow V_{O_2} = 1,95.22,4 = 43,68(lít)\)
Đúng 3
Bình luận (0)
PTHH: 2\(C_4H_{10}\) + 13\(O_2\) ---> 8\(CO_2\) + 10\(H_2O\) (Lập và cân bằng phương trình)
0,3 mol 1,95 mol 1,2 mol 1,5 mol
+ Số mol của \(C_4H_{10}\)
\(n_{C_4H_{10}}\) = \(\dfrac{V}{22,4}\) = \(\dfrac{6,72}{22,4}\) = 0,3 (mol)
+ Thể tích \(O_2\) cần dùng:
\(V_{O_2}\) = n . 22,4 = 1,95 . 22,4 = 43,68 (lít)
______________________________________
Có gì không đúng nhắn mình nha bạn :))
Đúng 0
Bình luận (0)
a, Tính thể tích của oxi (đktc) cần dùng để đốt cháy hết 3,1 gam P, biết phản ứng sinh ra chất rắn P2O5.
b, Đốt cháy hoàn toàn 1,12 lít khí CH4 (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được sản phẩm là khí cacbonic (CO2) và nước (H2O). Giá trị của V là
a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn 8,96 lít khí butan c4h10 (đktc) thu đc m (g) khí cacbonic
a) tìm m
b) thể tích khí o2 (đktc) cần dùng cho phản ứng trên
c) nếu dùng lượng oxi trên vào bình chứ 9,1g photpho, đun nóng . tính khối lượng sản phẩm thu đc . gọi tên sản phẩm
giúp hộ mình cái mình đg cần gấp , mình cảm ơn
a) \(n_{C_4H_{10}}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2C4H10 + 13O2 --to--> 8CO2 + 10H2O
0,4---->2,6---------->1,6------->2
=> m = 1,6.44 = 70,4 (g)
b) \(V_{O_2}=2,6.22,4=58,24\left(l\right)\)
c) \(n_P=\dfrac{9,1}{31}=\dfrac{91}{310}\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
Xét tỉ lê \(\dfrac{\dfrac{91}{310}}{4}< \dfrac{2,6}{5}\) => P hết, O2 dư
\(m_{P_2O_5}=\dfrac{91}{620}.142=\dfrac{6461}{310}\left(g\right)\)
Tên sản phẩm: Điphotpho pentaoxit
Đúng 5
Bình luận (0)